Tembaga Daftar isi Sejarah | Karakteristik | Senyawa | Produksi | Aplikasi | Lihat pula | Referensi | Menu navigasisuntingChambers's Information for the PeopleEncyclopedia of applied physics"Copper.org: Education: Statue of Liberty: Reclothing the First Lady of Metals – Repair Concerns"10.1149/1.20484042003NuPhA.729....3A10.1016/j.nuclphysa.2003.11.001"Interactive Chart of Nuclides""Clinical Application and Quantitative Evaluation of Generator-Produced Copper-62-PTSM as a Brain Perfusion Tracer for PET"7989968astro-ph/07037602007MNRAS.378L..59R10.1111/j.1745-3933.2007.00320.xNature's building blocks: an A-Z guide to the elements"The largest crystals""The bioleaching of sulphide minerals with emphasis on copper sulphides — A review"10.1016/j.hydromet.2006.05.001716492542"Peak copper?"10.1111/j.1468-0289.1986.tb00411.x2596347"Copper Trends: Live Metal Spot Prices""A Bottom In Sight For Copper""International Copper Association""Overview of Recycled Copper" Copper.org"Copper""Copper, Chemical Element – Overview, Discovery and naming, Physical properties, Chemical properties, Occurrence in nature, Isotopes"s
Unsur kimiaLogam transisi
unsur kimiatabel periodiknomor atombahasa Latinkonduktorpanaslistrikunsurkorositimahperungguagen anti bakterifungisinutrienIrakSiprusZaman Perungguperakemasunsur golongan 11tabel periodikSsesiumemasosmiumverdigrisPatung Libertysulfidatembaga sulfidaisotopspinradioaktifparuh waktuisotop metastabilnomor massaβ-β+64Cuagen radiokontraschelateterapi radiasipelacak radioaktiftembaga nativekalkopiritkalkositazuritmalasittembaga(I) oksidakupritSemenanjung KeweenawMichiganpolikristalbilangan oksidasihalidaTembaga(I) oksidatembaga(II) oksidatembaga(I) sulfidatembaga monosulfidatembaga(I) kloridatembaga(I) bromidatembaga(I) iodidatembaga(II) fluoridatembaga(II) kloridatembaga(II) bromidadiekstraksiChuquicamataChileBingham Canyon MineEl Chino MineBritish Geological Surveyleaching in-situfroth flotationbioleachingflash smeltingdipanggangmatteInternational Resource Paneldireduksibilletingotaloikonduktor listriktransmisi tenaga listrikaluminiumpembangkit listriktransmisi tenagadistribusi tenagatelekomunikasielektronikperalatan listrikKawat listrikkonduktivitas listrikkorosiekspansi termalkonduktivitas termal
Tembaga
Loncat ke navigasi
Loncat ke pencarian
 Native copper (~4 cm in size) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nama, simbol | tembaga, Cu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /ˈkɒpər/ KOP-ər | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penampilan | merah-jingga metalik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tembaga di tabel periodik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 29 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Golongan, blok | golongan 11, blok-d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | periode 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | logam transisi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Bobot atom standar (±) (Ar) | 63.546(3) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Ar] 3d10 4s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
per kelopak | 2, 8, 18, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat fisika | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase | solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 1357.77 K (1084.62 °C, 1984.32 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik didih | 2835 K (2562 °C, 4643 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kepadatan mendekati s.k. | 8.94 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 8.02 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | 13.26 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 300.4 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 24.440 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | +1, +2, +3, +4 sedikit oksida basa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1.90 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | (artikel) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 128 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 132±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari van der Waals | 140 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat muka (fcc) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kecepatan suara batang ringan | (annealed) 3810 m/s (pada s.k.) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | 16.5 µm/(m·K) (suhu 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | 401 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitas listrik | 16.78 n Ω·m (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Arah magnet | diamagnetik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Young | 110–128 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Shear | 48 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Bulk | 140 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rasio Poisson | 0.34 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Mohs | 3.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Vickers | 369 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Brinell | 874 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7440-50-8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Isotop tembaga terstabil | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

Tembaga
Tembaga adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Cu dan nomor atom 29. Lambangnya berasal dari bahasa Latin Cuprum.Tembaga merupakan konduktor panas dan listrik yang baik. Selain itu unsur ini memiliki korosi yang cepat sekali. Tembaga murni sifatnya halus dan lunak, dengan permukaan berwarna jingga kemerahan. Tembaga dicampurkan dengan timah untuk membuat perunggu.
Ion Tembaga(II) dapat berlarut ke dalam air, di mana fungsi mereka dalam konsentrasi tinggi adalah sebagai agen anti bakteri, fungisi, dan bahan tambahan kayu. Dalam konsentrasi tinggi maka tembaga akan bersifat racun, tetapi dalam jumlah sedikit tembaga merupakan nutrien yang penting bagi kehidupan manusia dan tanaman tingkat rendah. Di dalam tubuh, tembaga biasanya ditemukan di bagian hati, otak, usus, jantung, dan ginjal.
Daftar isi
1 Sejarah
2 Karakteristik
2.1 Fisik
2.2 Kimia
2.3 Isotop
2.4 Keberadaan
3 Senyawa
3.1 Senyawa biner
4 Produksi
4.1 Metode
4.2 Cadangan
4.3 Daur ulang
5 Aplikasi
5.1 Kabel dan kawat
6 Lihat pula
7 Referensi
Sejarah |
Tembaga adalah salah satu logam yang sangat penting dan berperan besar dalam sejarah manusia dan termasuk logam yang pertama kali ditambang[1]. Tembaga sudah digunakan sejak 10.000 tahun yang lalu. Sebuah kalung tembaga yang ditemukan di Irak diperkirakan dibuat pada masa 9500 SM[2].
Tembaga (Cuprum) memperoleh namanya dari bahasa Latin, Cyprium, yang berasal dari nama pulau Siprus di mana ia pertama kali dihasilkan. Cyprium kemudian disingkat menjadi Cuprum.
Tembaga berperan besar dalam peradaban manusia terutama pada Zaman Perunggu (3000-1000 SM). Pada masa tersebut tembaga dipadukan dengan timah menjadi perunggu. Perunggu kemudian diolah menjadi berbagai macam peralatan, senjata, koin, instrumen musik dan perhiasan[1]. .
Karakteristik |
Fisik |

Sebuah cakram tembaga (kemurnian 99,5%) dibuat dengan continuous casting dan etching

Tembaga yang tepat berada pada titik lelehnya akan tetap berwarna merah muda.
Tembaga, perak, dan emas berada pada unsur golongan 11 pada tabel periodik dan mempunyai sifat yang sama: mempunyai satu elektron orbital-s pada kulit atom d dengan sifat konduktivitas listrik yang baik.
Sifat lunak tembaga dapat dijelaskan oleh konduktivitas listriknya yang tinggi (59,6×106 S/m) dan oleh karena itu juga mempunyai konduktivitas termal yang tinggi (kedua tertinggi) di antara semua logam murni pada suhu kamar.[3]
Bersama dengan sesium dan emas (keduanya berwarna kuning) dan osmium (kebiruan), tembaga adalah satu dari empat logam dengan warna asli selain abu-abu atau perak.[4] Tembaga murni berwarna merah-oranye dan menjadi kemerahan bila kontak dengan udara.[5]
Kimia |

Kawat tembaga murni (kiri) dan kawat tembaga teroksidasi (kanan).

Menara Timur dari Royal Observatory, Edinburgh. Perbedaan antara tembaga yang baru dipasang kembali tahun 2010 dengan warna tembaga asli tahun 1894 dapat terlihat jelas.
Tembaga tidak bereaksi dengan air, namun ia bereaksi perlahan dengan oksigen dari udara membentuk lapisan coklat-hitam tembaga oksida. Berbeda dengan oksidasi besi oleh udara, lapisan oksida ini kemudian menghentikan korosi berlanjut. Lapisan verdigris (tembaga karbonat) berwarna hijau dapat dilihat pada konstruksi-konstruksi dari tembaga yang berusia tua, seperti pada Patung Liberty.[6] Tembaga bereaksi dengan sulfida membentuk tembaga sulfida.[7]
Isotop |
Tembaga memiliki 29 isotop.63Cu dan 65Cu adalah isotop stabil, dengan persentase 63Cu adalah yang terbanyak di alam, sekitar 69%. Kedua isotop ini memiliki bilangan spin 3/2.[8] Isotop lainnya bersifat radioaktif, dengan yang paling stabil adalah 67Cu dengan paruh waktu 61,83 jam.[8] Tujuh isotop metastabil telah diidentifikasi, 68mCu adalah isotop dengan paruh waktu terpanjang, 3,8 menit. Isotop dengan nomor massa diatas 64 dapat meluruh dengan β-, sedangkan untuk nomor massa dibawah 64 meluruh dengan β+. 64Cu (paruh waktu 12,7 jam), meluruh dengan kedua cara.[9]
62Cu dan 64Cu memiliki banyak kegunaan.64Cu adalah agen radiokontras untuk gambar X-ray, bersama dengan chelate dapat digunakan untuk terapi radiasi kanker.62Cu digunakan pada 62Cu-PTSM yang merupakan pelacak radioaktif untuk tomografi emisi positron.[10]
Keberadaan |
Tembaga disintesis pada bintang masif[11] dan ada di kerak bumi dengan konsentrasi 50 bagian per juta (ppm),[12] atau dapat juga dalam bentuk tembaga native atau mineral dalam bentuk tembaga sulfida kalkopirit dan kalkosit, tembaga karbonat azurit dan malasit dan mineral tembaga(I) oksida kuprit.[3] Massa tembaga murni yang pernah ditemukan bermassa 420 ton, ditemukan tahun 1857 di Semenanjung Keweenaw di Michigan, AS.[12] Tembaga native merupakan polikristal, dengan kristal terbesar yang pernah diketahui berukuran 4.4×3.2×3.2 cm.[13]
Senyawa |

Contoh tembaga(I) oksida.
Tembaga membentuk banyak macam senyawa, biasanya dengan bilangan oksidasi +1 dan +2.[14]
Senyawa biner |
Seperti elemen lainnya, senyawa tembaga yang paling sederhana adalah senyawa biner (terdiri dari 2 elemen saja). Biner yang paling penting diantaranya oksida, sulfida, dan halida. Tembaga(I) oksida, tembaga(II) oksida, tembaga(I) sulfida, dan tembaga monosulfida merupakan contoh senyawa tembaga biner.
Untuk senyawa halida, yang dikenal diantaranya tembaga(I) klorida, tembaga(I) bromida, dan tembaga(I) iodida, juga tembaga(II) fluorida, tembaga(II) klorida, dan tembaga(II) bromida. Percobaan membuat tembaga(II) iodida ternyata menghasilkan tembaga iodida dan iodin:[14]
- 2 Cu2+ + 4 I− → 2 CuI + I2
Produksi |

Chuquicamata di Chile adalah salah satu penambangan tembaga terbuka terbesar di dunia.

Tren produksi dunia
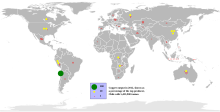
Produksi tembaga tahun 2005

Harga tembaga, 2003–2011 dalam dolar AS per ton
Kebanyakan tembaga ditambang atau diekstraksi dalam bentuk tembaga sulfida dari tambang terbuka atau deposit. Contoh tambang yang ada antara lain Chuquicamata di Chile, Bingham Canyon Mine di Utah, dan El Chino Mine di New Mexico, Amerika Serikat. Menurut British Geological Survey tahun 2005, Chile adalah produsen tembaga terbesar di dunia dan menguasai sepertiga pasar dunia, diikuti Amerika Serikat, Indonesia, dan Peru.[3] Tembaga juga dapat diperoleh dengan proses leaching in-situ. Beberapa kawasan tambang di Arizona menggunakan metode ini.[15]
Metode |
Konsentrasi tembaga pada bijih-bijih yang ada rata-rata hanya 0,6%, kebanyakan bijih komersial yang ada adalah sulfida seperti kalkopirit (CuFeS2) atau kalkosit (Cu2S).[16] Mineral ini ditingkatkan konsentrasi tembaganya sampai 10-15% dengan proses froth flotation atau bioleaching.[17] Memanaskan material ini dengan silika pada flash smelting akan melepaskan kandungan besi dan mengubah besi sulfida menjadi oksidanya. Senyawa produk copper matte yang terdiri dari Cu2S kemudian dipanggang untuk mengubah sulfida menjadi oksida:[16]
- 2 Cu2S + 3 O2 → 2 Cu2O + 2 SO2
Kuprat oksida kemudian dipanaskan:
- 2 Cu2O → 4 Cu + O2
Proses matte hanya mengkonversi setengah sulfida menjadi oksida dan kemudian menghilangkan semua sulfur menjadi oksida. Proses ini akan mengubah oksida tembaga menjadi logam tembaga. Gas alam kemudian dialirkan untuk menghilangkan oksigen (proses electrorefining) untuk kemudian mengubah material menjadi tembaga murni:[18]
- Cu2+ + 2 e– → Cu
Cadangan |
Tembaga telah digunakan sejak 10.000 tahun yang lalu, tetapi lebih dari 96% dari jumlah yang ditambang baru diekstraksi setelah 1900. Cadangan tembaga di bumi pun masih amat besar (sekitar 1014 ton), atau cukup untuk 5 juta tahun dengan kecepatan ekstraksi saat ini. Meski begitu, hanya sebagian kecil saja dari jumlah ini yang bernilai ekonomis, dengan teknologi dan harga jual saat ini. Beberapa estimasi mengatakan bahwa cadangan yang ada hanya cukup untuk 25 sampai 60 tahun lagi, tergantung dari seberapa besar peningkatan penggunaannya.[19] Daur ulang tembaga merupakan salah satu sumber utama.[20]
Harga tembaga juga tidak stabil,[21] misalnya dari harga US$0,60/lb (US$1,32/kg) bulan Juni 1999 menjadi US$3,75/lb (US$8,27/kg) bulan Mei 2006. Pada bulan Februari 2007, harganya turun lagi sampai US$2,40/lb (US$5,29/kg) dan kembali naik menjadi US$3,50/lb (US$7,71/kg) pada bulan April tahun yang sama.[22] Pada Februari 2009, permintaan dunia yang melemah dan kejatuhan berbagai harga komoditas menjadikan harga tembaga berkisar US$1,51/lb.[23]
Daur ulang |
Tembaga, seperti aluminium, dapat didaur ulang 100% tanpa mengurangi kualitasnya. Dilihat dari volumenya, tembaga adalah logam paling banyak ketiga yang didaur ulang, setelah besi dan aluminium. Diperkirakan bahwa 80% dari seluruh tembaga yang pernah ditambang masih digunakan saat ini.[24] Menurut laporan International Resource Panel, pemakaian tembaga per kapita global adalah sekitar 35–55 kg. Pemakai terbesarnya adalah negara-negara maju (140–300 kg per kapita) sedangkan di negara-negara berkembang sekitar 30–40 kg per kapita.
Proses daur ulang tembaga pada umumnya sama dengan proses ekstraksi, namun prosesnya lebih sedikit. Tembaga bekas dengan kemurnian tinggi dilelehkan di furnace dan kemudian direduksi dan dibentuk kembali menjadi billet dan ingot; sedangkan tembaga bekas dengan kemurnian lebih rendah diproses ulang dengan electroplating di dalam asam sulfat.[25]
Aplikasi |

Assorted copper fittings
Penggunaan tembaga terbesar adalah untuk kabel listrik (60%), atap dan perpipaan (20%) dan mesin industri (15%). Tembaga biasanya digunakan dalam bentuk logam murni, tetapi ketika dibutuhkan tingkat kekerasan lebih tinggi maka biasanya dicampur dengan elemen lain untuk membentuk aloi.[12] Sebagian kecil tembaga juga digunakan sebagai suplemen nutrisi dan fungisida dalam pertanian.[26][27]
Kabel dan kawat |
Meski bersaing dengan material lainnya, tembaga tetap dipilih sebagai konduktor listrik utama di hampir semua kategori kawat listrik kecuali di bagian transmisi tenaga listrik di mana aluminium lebih dipilih.[28][29] Kawat tembaga digunakan untuk pembangkit listrik, transmisi tenaga, distribusi tenaga, telekomunikasi, sirkuit elektronik, dan berbagai macam peralatan listrik lainnya.[30]Kawat listrik adalah pasar paling penting bagi industri tembaga.[31] Hal ini termasuk kabel pada gedung, kabel telekomunikasi, kabel distribusi tenaga, kabel otomotif, kabel magnet, dsb. Setengah dari jumlah tembaga yang ditambang digunakan untuk membuat kabel listrik dan kabel konduktor.[32] Banyak alat listrik menggunakan kawat tembaga karena memiliki konduktivitas listrik tinggi, tahan korosi, ekspansi termal rendah, konduktivitas termal tinggi, dapat disolder, dan mudah dipasang.
Lihat pula |
- Tumbaga
Referensi |
^ abParsons, Paul. "Copper". Dalam Dixon, Gail. The Periodic Table - A Field Guide to The Eleements. Quercus. hlm. 74. ISBN 978-1-78087-327-5.
^ Coulson, Michael. "Appendix". The History of Mining - The Events, Technology and People Involved in the Industry that Forged Modern World. Harriman House. hlm. 427. ISBN 978-1897597903.
^ abcHammond, C. R. (2004). The Elements, in Handbook of Chemistry and Physics 81st edition. CRC press. ISBN 0-8493-0485-7.
^ Chambers, William; Chambers, Robert (1884). Chambers's Information for the People. L (edisi ke-5th). W. & R. Chambers. hlm. 312. ISBN 0-665-46912-8.
^ George L. Trigg; Edmund H. Immergut (1 November 1992). Encyclopedia of applied physics. 4: Combustion to Diamagnetism. VCH Publishers. hlm. 267–272. ISBN 978-3-527-28126-8. Diakses tanggal 2011-05-02.
^ "Copper.org: Education: Statue of Liberty: Reclothing the First Lady of Metals – Repair Concerns". Copper.org. Diakses tanggal 2011-04-11.
^ Rickett, B. I.; Payer, J. H. (1995). "Composition of Copper Tarnish Products Formed in Moist Air with Trace Levels of Pollutant Gas: Hydrogen Sulfide and Sulfur Dioxide/Hydrogen Sulfide". Journal of the Electrochemical Society. 142 (11): 3723–3728. doi:10.1149/1.2048404.
^ abAudi, G; Bersillon, O.; Blachot, J.; Wapstra, A.H. (2003). "Nubase2003 Evaluation of Nuclear and Decay Properties". Nuclear Physics A. Atomic Mass Data Center. 729: 3. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
^ "Interactive Chart of Nuclides". National Nuclear Data Center. Diakses tanggal 2011-04-08.
^ Okazawa, Hidehiko; et al. (1994). "Clinical Application and Quantitative Evaluation of Generator-Produced Copper-62-PTSM as a Brain Perfusion Tracer for PET" (PDF). Journal of Nuclear Medicine. 35 (12): 1910–1915. PMID 7989968. Parameter|first2=tanpa|last2=di Authors list (bantuan); Parameter|first3=tanpa|last3=di Authors list (bantuan); Parameter|first4=tanpa|last4=di Authors list (bantuan); Parameter|first5=tanpa|last5=di Authors list (bantuan); Parameter|first6=tanpa|last6=di Authors list (bantuan); Parameter|first7=tanpa|last7=di Authors list (bantuan); Parameter|first8=tanpa|last8=di Authors list (bantuan); Parameter|first9=tanpa|last9=di Authors list (bantuan); Parameter|first10=tanpa|last10=di Authors list (bantuan)Pemeliharaan CS1: Penggunaan et al. yang eksplisit (link)
^ Romano, Donatella; Matteucci, Fransesca (2007). "Contrasting copper evolution in ω Centauri and the Milky Way". Monthly Notices of the Royal Astronomical Society: Letters. 378 (1): L59–L63. arXiv:astro-ph/0703760 . Bibcode:2007MNRAS.378L..59R. doi:10.1111/j.1745-3933.2007.00320.x.
. Bibcode:2007MNRAS.378L..59R. doi:10.1111/j.1745-3933.2007.00320.x.
^ abcEmsley, John (11 August 2003). Nature's building blocks: an A-Z guide to the elements. Oxford University Press. hlm. 121–125. ISBN 978-0-19-850340-8. Diakses tanggal 2011-05-02.
^ Rickwood, P. C. (1981). "The largest crystals" (PDF). American Mineralogist. 66: 885.
^ abHolleman, A. F.; Wiberg, N. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 978-0-12-352651-9.
^ http://www.azcentral.com/arizonarepublic/business/articles/2011/06/19/20110619copper-new-method-fight.html
^ abGreenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2nd), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4 Pemeliharaan CS1: Banyak nama: authors list (link)
^ Watling, H. R. (2006). "The bioleaching of sulphide minerals with emphasis on copper sulphides — A review" (PDF). Hydrometallurgy. 84 (1, 2): 81–108. doi:10.1016/j.hydromet.2006.05.001.
^ Samans, Carl (1949). Engineering metals and their alloys. New York: Macmillan. OCLC 716492542.
^ Brown, Lester (2006). Plan B 2.0: Rescuing a Planet Under Stress and a Civilization in Trouble. New York: W.W. Norton. hlm. 109. ISBN 0-393-32831-7.
^ Leonard, Andrew (2006-03-02). "Peak copper?". Salon – How the World Works. Diakses tanggal 2008-03-23.
^ Schmitz, Christopher (1986). "The Rise of Big Business in the World, Copper Industry 1870–1930". Economic History Review. 2. 39 (3): 392–410. doi:10.1111/j.1468-0289.1986.tb00411.x. JSTOR 2596347.
^ "Copper Trends: Live Metal Spot Prices".
^ Ackerman, R. (2 April 2009). "A Bottom In Sight For Copper". Forbes.
^ "International Copper Association".
^ "Overview of Recycled Copper" Copper.org. Copper.org (2010-08-25). Retrieved on 2011-11-08.
^ Kesalahan pengutipan: Tag<ref>tidak sah;
tidak ditemukan teks untuk ref bernamaBoux
^ "Copper". American Elements. 2008. Diakses tanggal 2008-07-12.
^ Pops, Horace, 2008, Processing of wire from antiquity to the future, Wire Journal International, June, pp 58–66
^ The Metallurgy of Copper Wire, http://www.litz-wire.com/pdf%20files/Metallurgy_Copper_Wire.pdf
^ Joseph, Günter, 1999, Copper: Its Trade, Manufacture, Use, and Environmental Status, edited by Kundig, Konrad J.A., ASM International, pps. 141–192 and pps. 331–375.
^ "Copper, Chemical Element – Overview, Discovery and naming, Physical properties, Chemical properties, Occurrence in nature, Isotopes". Chemistryexplained.com. Diakses tanggal 2012-10-16.
^ Joseph, Günter, 1999, Copper: Its Trade, Manufacture, Use, and Environmental Status, edited by Kundig, Konrad J.A., ASM International, p.348
Tabel periodik (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
1 | H | He | |||||||||||||||||||||||||||||||
2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
Kategori:
- Unsur kimia
- Logam transisi
(window.RLQ=window.RLQ||[]).push(function()mw.config.set("wgPageParseReport":"limitreport":"cputime":"1.452","walltime":"1.736","ppvisitednodes":"value":35792,"limit":1000000,"ppgeneratednodes":"value":0,"limit":1500000,"postexpandincludesize":"value":397585,"limit":2097152,"templateargumentsize":"value":28874,"limit":2097152,"expansiondepth":"value":22,"limit":40,"expensivefunctioncount":"value":0,"limit":500,"unstrip-depth":"value":0,"limit":20,"unstrip-size":"value":33755,"limit":5000000,"entityaccesscount":"value":1,"limit":400,"timingprofile":["100.00% 1298.779 1 -total"," 39.33% 510.856 1 Templat:Kotak_info_tembaga"," 38.95% 505.872 1 Templat:Elementbox"," 38.15% 495.433 2 Templat:Infobox"," 36.69% 476.533 1 Templat:Compact_periodic_table"," 30.65% 398.011 118 Templat:Element_cell-compact"," 27.74% 360.241 134 Templat:Element_color"," 17.95% 233.145 1 Templat:Reflist"," 14.96% 194.251 1 Templat:Infobox_element/periodic_table"," 13.06% 169.571 1 Templat:Periodic_table_(32_columns,_micro)"],"scribunto":"limitreport-timeusage":"value":"0.482","limit":"10.000","limitreport-memusage":"value":6373816,"limit":52428800,"cachereport":"origin":"mw1270","timestamp":"20190322103430","ttl":2592000,"transientcontent":false);mw.config.set("wgBackendResponseTime":151,"wgHostname":"mw1271"););